Anvisa libera medicamento para o SUS contra a perda da visão

A Agência Nacional de Vigilância Sanitária (Anvisa) concedeu autorização de uso excepcional do medicamento bevacizumabe (Avastin) na rede pública de saúde. A Resolução da Diretoria Colegiada de número 111 foi publicada no Diário Oficial da União (DOU) da última quarta-feira, 8 de setembro.
O Avastin/bevacizumabe tem registro na Anvisa desde 2002 como medicamento oncológico para o tratamento do carcinoma metastásico. Mas não há registro desse remédio para uso oftalmológico na Anvisa ou em outra agência internacional.
Ao longo dos anos observou-se que o bevacizumabe tem ação efetiva no tratamento de doenças provocadas pelo crescimento anormal de vasos sanguíneos na retina, controlando o Fator de Crescimento Endotelial Vascular humano A (VEGF-A), presente na retina.
Por sua ação Anti-VEGF, o bevacizumabe já é utilizado em outros países com efetividade para tratar a Degeneração Macular Relacionada à Idade (DMRI), doença que acomete a população a partir dos 50 anos, sendo mais frequente a partir dos 65 anos.
Inclusão no SUS
A decisão da Anvisa atende à uma solicitação de autorização de uso feita pela Comissão Nacional de Incorporação de Tecnologias no SUS (Conitec) do Ministério da Saúde à Agência, com base nos estudos científicos sobre o efeito do bevacizumabe na DMRI.
O uso excepcional solicitado pelo Ministério da Saúde (MS), está previsto no Artigo 21 do Decreto 8.077, de 14 de agosto de 2013. Atualmente, o medicamento é usado para DMRI em muitos países como Tailândia, EUA, Itália, França e também no Brasil.
A autorização dada pela Anvisa tem duração de três anos, renovável por igual período. Na RDC 111/2016, a agência estabeleceu as exigências sanitária às quais estão condicionadas o uso do medicamento.
Últimas notícias

Marcelo Beltrão destaca fortalecimento dos municípios durante a XXVII Marcha em Brasília

Trabalho de Rafael Brito garante reajuste automático do piso do magistério para todos os professores

Projeto de Cabo Bebeto aprovado na ALE obriga escolas a comunicar pais sobre atividades de gênero
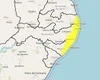
Semarh divulga previsão do tempo para esta quarta-feira (20) em Alagoas

Ação do prefeito Ronaldo Lopes reduz pela metade taxas anuais para taxistas e mototaxistas de Penedo

Charles Pacheco participa de Marcha Municipalista em busca de avanços para São Sebastião
Vídeos e noticias mais lidas

Publicado edital para o concurso do Detran; veja cargos e salários

Jovem é expulso após ser flagrado se masturbando dentro de academia de Arapiraca

Jovem morre após complicações de dengue hemorrágica em Arapiraca

Com avanço das obras, novo binário de Arapiraca já recebe sinalização e mobiliários urbanos

