CoronaVac: diretor do Butantan diz que interrupção não afetou estudo
Comissão do Congresso convocou representantes do instituto e da Anvisa
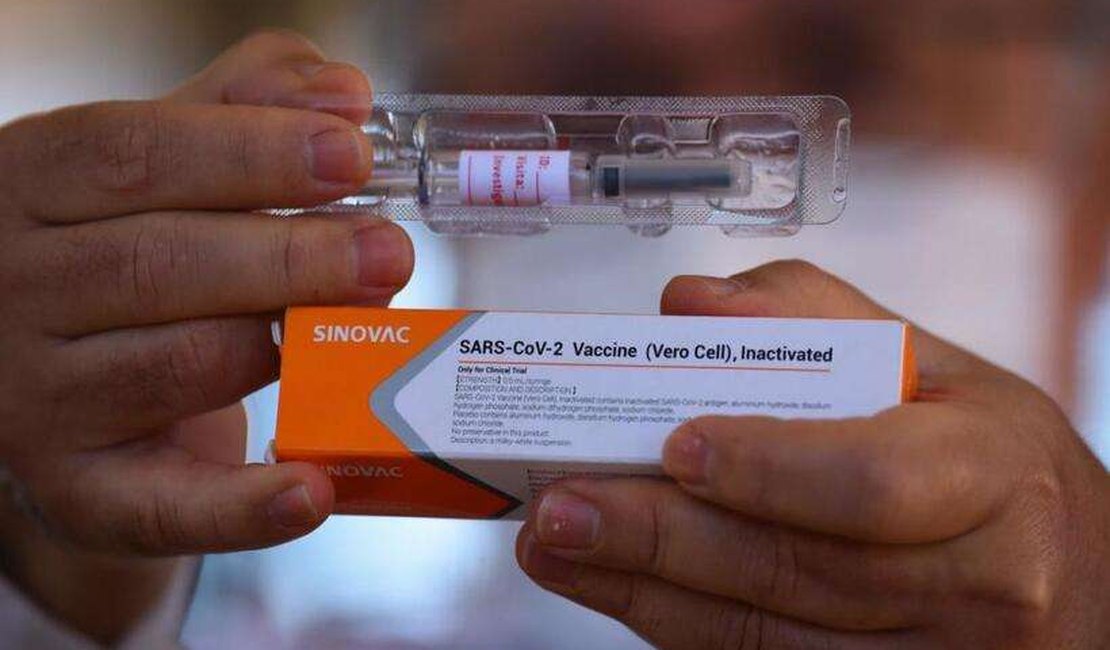
O diretor do Instituto Butantan, Dimas Tadeu Covas, afirmou nesta sexta-feira (13), na comissão mista do Congresso Nacional, que a interrupção dos estudos da vacina CoronaVac, feitos em parceria com o laboratório chinês Sinovac, "não teve efeito prático nenhum" e que a única questão que sobra desse incidente é política.
Dimas Covas afirmou que a comunicação entre o Butantan e a Anvisa (Agência Nacional de Vigilância Sanitária) , responsável por suspender na segunda-feira (9) a pesquisa do imunizante contra a covid-19, se deu no prazo correto e com todos os dados necessários. Dois dias depois, o estudo foi retomado.
Ele também declarou que não partiu do instituto as informações sobre a causa da morte do paciente que fazia parte do estudo. Na terça-feira, a imprensa divulgou que tratava-se de um homem em São Paulo, que se matou, sem nenhuma relação da morte com o imunizante testado para a covid-19.
Dimas Covas afirmou que a Coronavac já foi ministrada mais de 18 mil vezes no Brasil, a mais de 10 mil voluntários. Na China, país de origem do medicamento, mais de 70 mil pessoas foram. "De todas elas [vacinas testadas contra a covid-19], essa é a que tem o melhor perfil de segurança", afirmou "Isso até pela tecnologia usada, uma vacina baseada no vírus inativada", acrescentou.
O diretor do Butantan afrimou que até meados de janeiro o Brasil já deve ter 46 milhões de doses da vacina disponíveis. Seis milhões devem chegar agora no dia 20 e as outras 40 milhões serão produzidas aqui no país.
Comunicação falha e surpresa
Ele explicou que a interrupção se deu por falha de comunicação na segunda-feira. De acordo com ele, os comitês de ética do Butantan não viram qualquer problema no evento adverso descoberto que pudesse levar à paralisação do estudo.
"O Butantan fez a notificação do ocorrido à Anvisa dentro do prazo, e por algum motivo esse aviso teve problemas no sistema da Anvisa, por causa da invasão."
No dia 9 [segunda-feira], às 15h, explicou Dimas Covas, a Anvisa pediu que o Butantan encaminhasse todas as notificações de eventos adversos em no máximo um dia. Às 18h do mesmo dia, a agência pediu para encaminhar rapidamente a documentação. "Mandamos e ficamos aguardando. Era umas 8h47 da noite quando os membros que compõem a equipe técnica do estudo no Butantan receberam um convite para uma reunião emergencial no dia 10 para tratar de assuntos relacionados às notficiações."
"E pouco mais tarde fomos surpreendidos pela notícia de que o estudo clínico havia sido suspenso dada a gravidade do efeito adverso. Esses são os fatos."
Veja também
Últimas notícias

Palmeira dos Índios é única cidade de Alagoas a receber Prêmio de Inclusão Socioeconômica em Brasília

Penedo sedia encontro nacional dos Conselhos Municipais de Educação

Famílias de São Sebastião são beneficiadas com títulos de propriedade de imóveis

PL de Renan Calheiros avança no Senado com linha de crédito especial para produtores rurais endividados

Polícia desmancha depósito e apreende mais de 18kg de drogas no bairro São Luiz em Arapiraca

João Vicente explica escolha de Tino Marcos para novo projeto do Porta
Vídeos e noticias mais lidas

Publicado edital para o concurso do Detran; veja cargos e salários

Jovem é expulso após ser flagrado se masturbando dentro de academia de Arapiraca

Após demissão de Moro, Bolsonaro fará declaração às 17h

Mototaxista é assassinado a tiros em São Luís do Quitunde